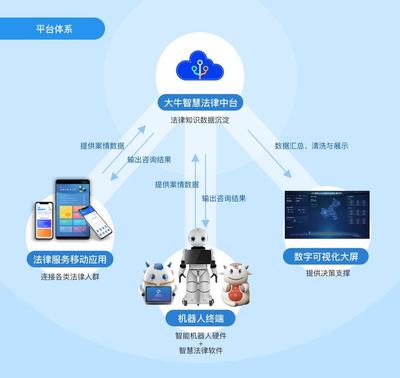
人工智能医疗器械监管现状与公共服务技术咨询服务
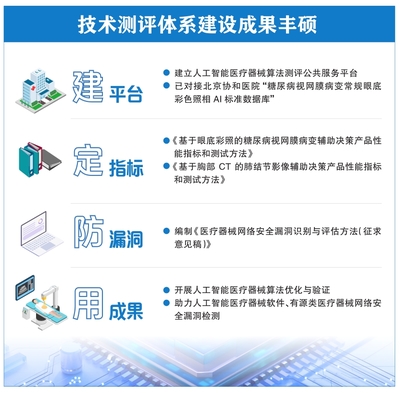
随着人工智能(AI)技术在医疗领域的广泛应用,AI医疗器械已成为推动精准医疗、提升诊疗效率的重要工具。其快速迭代与复杂性也给监管带来了前所未有的挑战。与此为促进行业健康、合规发展,专业的公共服务技术咨询服务应运而生,成为连接创新、监管与市场落地的关键桥梁。
一、全球与中国AI医疗器械监管现状
1. 全球监管框架逐步建立
各国监管机构正积极应对AI医疗器械带来的新问题。例如,美国食品药品监督管理局(FDA)通过“数字健康预认证计划”等创新路径,对AI软件作为医疗器械(SaMD)进行分类审批;欧盟则在新版《医疗器械法规》(MDR)中强化了对AI算法的临床评价与持续监测要求。国际医疗器械监管机构论坛(IMDRF)也发布了多项指导文件,致力于推动全球监管协同。
2. 中国监管体系日趋完善
中国国家药品监督管理局(NMPA)高度重视AI医疗器械的监管。目前已发布《深度学习辅助决策医疗器械软件审评要点》等关键文件,明确了AI医疗器械的注册审批路径。监管重点聚焦于算法性能、数据质量、临床验证及网络安全等方面,并强调“软件即医疗设备”的全生命周期管理理念。AI医疗器械按风险等级分为三类,其中第三类高风险产品需进行严格临床试验与审批。
3. 监管挑战与趋势
AI医疗器械的“自学习”特性使其在上市后可能持续演化,这对传统静态监管模式构成挑战。当前监管趋势正朝着动态监管、实时监测与算法透明度方向发展,强调通过真实世界数据(RWD)进行持续性能评估。数据隐私、算法偏见与伦理问题也成为全球监管关注的焦点。
二、人工智能公共服务技术咨询服务的价值与内容
面对复杂的监管环境与技术门槛,专业的AI医疗器械公共服务技术咨询服务显得尤为重要。这类服务通常由政府支持平台、行业协会或第三方专业机构提供,旨在降低企业合规成本,加速产品上市。
1. 核心服务内容
- 法规与标准解读:提供国内外最新监管政策、标准(如ISO、IEC标准)的深入解读与合规指导。
- 产品注册咨询:协助企业完成从分类界定、检测检验、临床评价到注册申报的全流程规划。
- 技术评估与测试支持:包括算法性能验证、数据质量管理体系构建、网络安全测试等。
- 全生命周期管理咨询:涵盖上市后监测、软件更新管理、不良事件报告等持续合规服务。
- 培训与交流平台:组织行业研讨会、专家培训,促进产学研医管各方交流。
2. 服务价值体现
- 降低合规风险:帮助企业精准理解并满足监管要求,避免因不合规导致的上市延迟或召回。
- 加速创新转化:通过专业指导优化研发与验证流程,缩短产品从实验室走向临床的时间。
- 促进行业生态建设:搭建公开、透明的咨询服务平台,增强行业互信,推动高质量协同发展。
三、展望:构建协同共治的健康发展生态
AI医疗器械的监管与服务将更加强调“智慧监管”与“创新服务”并重。一方面,监管机构有望借助AI技术自身提升监管效能,实现更精准的风险预警;另一方面,公共服务技术咨询将向专业化、精细化、国际化纵深发展,形成覆盖研发、注册、上市后各环节的服务网络。
对于企业与开发者而言,主动融入监管框架、积极利用公共服务资源,是确保产品安全有效、赢得市场信任的必由之路。只有通过监管、服务与创新的良性互动,才能充分释放AI在医疗领域的巨大潜力,最终造福于全球患者。
最新产品